La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), informa sobre la autorización para uso de emergencia de dos lotes de vacunas envasados en México para la prevención de COVID-19.
El primer lote liberado fue envasado en el Estado de México por Laboratorios Liomont, S.A. de C.V., y contiene 914 mil 200 dosis del biológico AstraZeneca. El segundo, envasado en Querétaro por la farmacéutica Drugmex, S.A.P.I. de C.V., corresponde a CanSino Biologics con 151 mil 860 dosis de la vacuna.
Una vez liberados, ambos se destinan a la Política Nacional de Vacunación contra el virus SARS-CoV-2, para la prevención de COVID-19 en México, disponible en https://bit.ly/3tNfUzL, y son susceptibles de ser enviados a otros países como parte de algún acuerdo con los fabricantes.
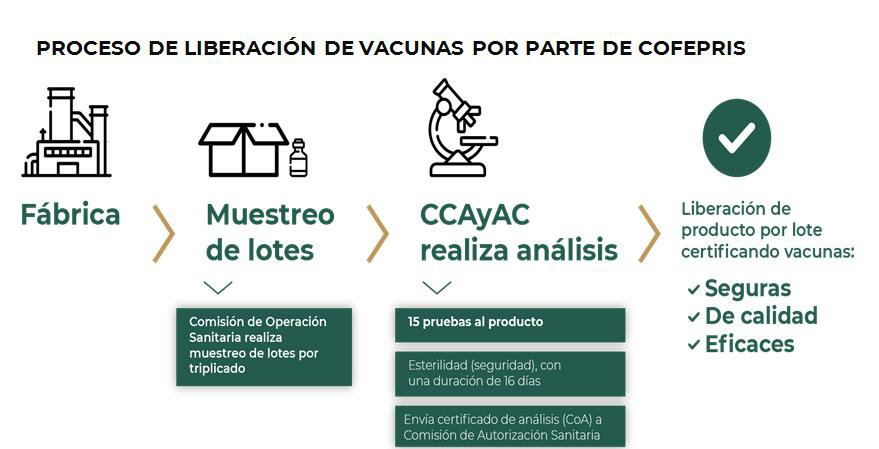
La autorización para uso de emergencia se emite después de realizar las pruebas necesarias a través del Laboratorio Nacional de Referencia de la Comisión de Control Analítico y Ampliación de Cobertura, donde se realizaron 15 pruebas a los biológicos contra COVID-19, como esterilidad, identidad y potencia, entre otras.
En total se han liberado 6 millones 544 mil 900 dosis de la vacuna AstraZeneca y 4 millones 910 mil 060 dosis de la vacuna CanSino Biologics. El total de liberaciones para uso de emergencia de ambos biológicos envasados en México es de 29 lotes con 11 millones 454 mil 960 dosis.
La población puede confiar en que todas las vacunas aprobadas por esta comisión son seguras y eficaces, y que deben ser aplicadas de manera gratuita y universal siguiendo el plan de vacunación establecido por la Secretaría de Salud.


